Gambar Pool / Pool / Getty
Poin Penting
- FDA memberikan otorisasi penggunaan darurat untuk vaksin COVID-19 yang dikembangkan oleh Pfizer dan BioNTech.
- Berita itu muncul sehari setelah komite penasihat FDA merekomendasikan badan tersebut mengesahkan vaksin
- Data yang ditinjau oleh panitia menemukan vaksin 95% efektif.
- Distribusi vaksin bisa datang dalam waktu 24 jam setelah otorisasi.
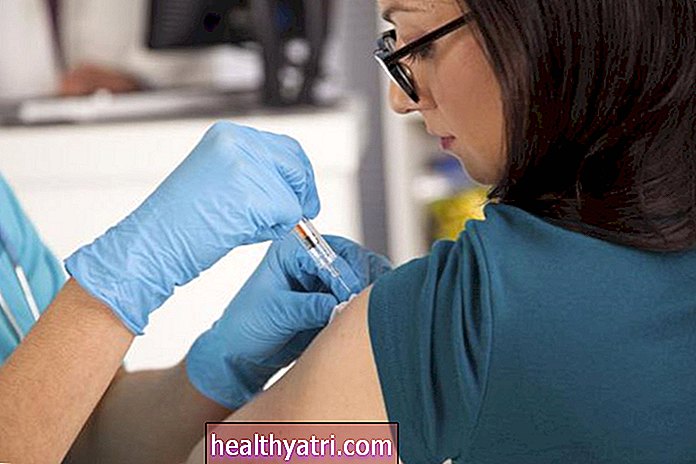
Badan Pengawas Obat dan Makanan (FDA) memberikan otorisasi penggunaan darurat untuk vaksin COVID-19 pertamanya pada Jumat malam. Vaksin yang dikembangkan oleh Pfizer Inc. dan perusahaan Jerman BioNTech akan segera mulai didistribusikan.
Berita tersebut mengikuti audiensi publik yang sangat dinantikan pada hari Kamis, di mana panel penasihat FDA memberikan suara 17-4 mendukung otorisasi vaksin Pfizer, dengan satu abstain.
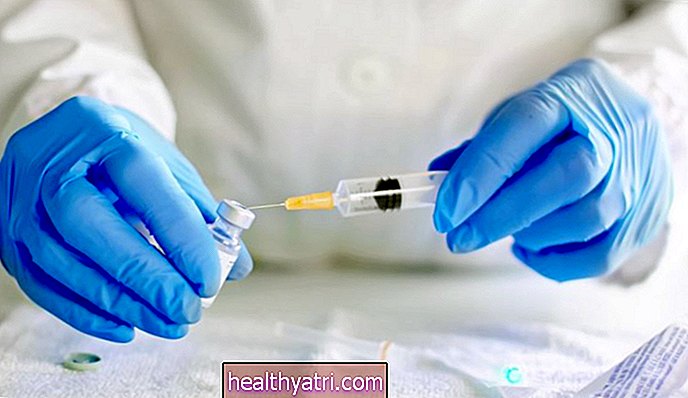
Pfizer mempresentasikan data dari uji klinis yang melibatkan 43.000 peserta dewasa. Awal pekan ini, FDA membagikan beberapa data tersebut, termasuk fakta bahwa 95% orang dalam uji klinis yang menerima vaksin tidak terus mengembangkan COVID. -19. Efek sampingnya ringan, termasuk menggigil, nyeri ringan, dan kemerahan di tempat suntikan.
Otorisasi penggunaan darurat (EUA) berlaku untuk orang yang berusia 16 tahun ke atas. Pfizer juga melakukan uji klinis tentang keamanan dan kemanjuran vaksin pada anak-anak berusia 12 tahun, dan diharapkan dapat menambah uji coba untuk anak-anak yang lebih kecil.
Data Keamanan dan Khasiat Dari Lebih Banyak Penduduk Masih Dibutuhkan
Panel penasihat FDA, yang disebut Komite Penasihat Vaksin dan Produk Biologi Terkait (VRBPAC), merekomendasikan Pfizer mengambil tindakan tambahan untuk memastikan vaksinnya aman dan efektif untuk lebih banyak populasi. Panel menyarankan agar lebih banyak orang kulit berwarna ditambahkan ke uji klinis yang sedang berlangsung. Orang kulit berwarna lebih mungkin daripada orang kulit putih untuk tertular COVID-19 dan meninggal karena virus.
Panel juga membahas dua kasus reaksi alergi yang dilaporkan pada orang yang menerima vaksin di Inggris minggu ini, yang telah disetujui. Paul Offit, MD, direktur Pusat Pendidikan Vaksin di Rumah Sakit Anak Philadelphia, bertanya kepada presenter Pfizer tentang reaksi alergi, khawatir orang dengan alergi parah mungkin memilih untuk tidak menggunakan vaksin. Offit merekomendasikan agar penelitian juga dilakukan pada vaksin pada orang dengan alergi umum.
Inggris Raya merekomendasikan orang dengan riwayat anafilaksis ke obat atau makanan untuk tidak mendapatkan vaksin. A.S. dapat menambahkan peringatan serupa bersamaan dengan otorisasi. Staf FDA pada pertemuan tersebut mengatakan kepada panel bahwa mereka sudah mengerjakan dokumentasi tertulis untuk konsumen tentang keamanan dan efektivitas vaksin.
Apa Artinya Ini Untuk Anda
Berdasarkan rekomendasi dari komite penasihat untuk mengotorisasi vaksin COVID-19 Pfizer, Food and Drug Administration dapat menyetujui penggunaannya dalam beberapa hari. Distribusi dapat dimulai segera setelah itu.Dosis pertama vaksin diharapkan diberikan kepada petugas kesehatan dan penghuni panti jompo.
Menyusul keputusan VRBPAC, komisaris FDA Stephen M.Hahn, MD mengeluarkan pernyataan:
“Biasanya, proses peninjauan vaksin yang dipelajari pada puluhan ribu orang membutuhkan waktu berbulan-bulan. Meskipun proses telah dipercepat sehubungan dengan tinjauan EUA ini, staf peninjau ahli FDA telah meninjau ribuan halaman informasi teknis [termasuk] data uji klinis, data non-klinis tentang pengembangan vaksin di laboratorium, dan membuat data tentang bagaimana vaksin dibuat. "
Hahn, yang mungkin berusaha untuk menghilangkan ketakutan di antara konsumen, menambahkan: “Di masa yang sangat mendesak ini, staf FDA merasa bertanggung jawab untuk bergerak secepat mungkin melalui proses peninjauan. Namun, mereka tahu bahwa mereka harus menjalankan mandat mereka untuk melindungi kesehatan masyarakat dan untuk memastikan bahwa setiap vaksin resmi memenuhi standar ketat kami untuk keamanan dan efektivitas yang diharapkan masyarakat Amerika. ”
Presiden terpilih Joe Biden juga mengeluarkan pernyataan setelah pemungutan suara komite yang mengatakan, "integritas sains membawa kami ke titik ini."
FDA mengatakan bahwa distribusi vaksin dapat dilakukan dalam waktu 24 jam setelah otorisasi.
Komite penasihat FDA akan meninjau vaksin COVID-19 kedua, yang dibuat oleh Moderna, pada Kamis, 17 Desember.