Poin Penting
- Administrasi Makanan dan Obat (FDA) telah mengeluarkan otorisasi penggunaan darurat (EUA) dari perawatan antibodi virus korona yang dibuat oleh Eli Lilly.
- Koktail antibodi disebut bamlanivimab dan telah diizinkan untuk digunakan pada pasien berisiko tinggi yang baru didiagnosis berusia 12 tahun ke atas.
- Eli Lilly mengatakan pihaknya berencana untuk memproduksi hingga satu juta dosis bamlanivimab pada akhir tahun 2020.
Badan Pengawas Obat dan Makanan (FDA) mengumumkan dalam sebuah surat pada hari Senin bahwa mereka akan mengeluarkan otorisasi penggunaan darurat (EUA) dari perawatan antibodi penawar COVID-19 yang dibuat oleh perusahaan farmasi Eli Lilly.
"Otorisasi darurat ini memungkinkan kami menyediakan pengobatan COVID-19 untuk pasien berisiko tinggi yang baru saja didiagnosis - menambahkan alat yang berharga bagi dokter yang memerangi beban pandemi global yang kini semakin meningkat," Dave Ricks, ketua dan CEO Eli Lilly, kata dalam rilis berita.
Kemungkinan pengobatan yang layak datang pada saat COVID-19 menginfeksi lebih dari 140.000 orang per hari.
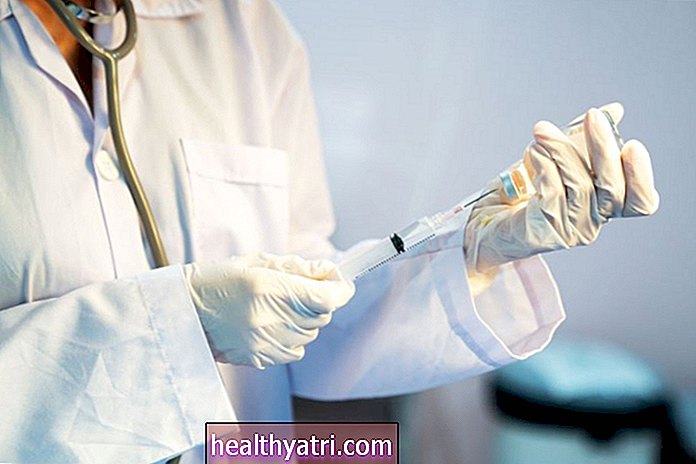
Perawatan, yang disebut bamlanivimab (LY-CoV555), telah diizinkan untuk pengobatan COVID-19 ringan hingga sedang pada orang dewasa dan anak-anak 12 tahun ke atas dengan tes COVID-19 positif, dan yang berisiko tinggi berkembang menjadi parah. COVID-19 dan / atau rawat inap, menurut pernyataan perusahaan. Koktail antibodi harus diberikan sebagai infus intravena tunggal dalam 10 hari setelah timbulnya gejala COVID-19.
“Seperti yang diilustrasikan oleh tindakan hari ini, FDA tetap berkomitmen untuk mempercepat pengembangan dan ketersediaan perawatan COVID-19 potensial dan memberikan pasien yang sakit akses tepat waktu ke terapi baru jika sesuai, sementara pada saat yang sama mendukung penelitian untuk mengevaluasi lebih lanjut apakah mereka aman dan efektif, ”Komisaris FDA Stephen M. Hahn, MD, mengatakan dalam rilis berita 9 November. “Melalui Program Percepatan Perawatan Virus Corona kami, FDA terus bekerja sepanjang waktu dan menggunakan setiap alat yang kami miliki untuk upaya ini.”
Berita Eli Lilly diumumkan pada hari yang sama Pfizer mengatakan telah memperoleh hasil awal yang positif dari uji coba vaksin Fase 3. Tetapi Pfizer mengatakan dalam sebuah pernyataan bahwa bahkan dengan EUA yang disetujui, mereka tidak akan dapat memberikan sebagian besar dosis yang tersedia hingga 2021.
Eli Lilly mengatakan pihaknya berencana untuk memproduksi hingga satu juta dosis bamlanivimab pada akhir tahun 2020.
Patrizia Cavazzoni, MD
"Otorisasi darurat FDA atas bamlanivimab memberi para profesional perawatan kesehatan di garis depan pandemi ini dengan alat potensial lain dalam merawat pasien COVID-19."
- Patrizia Cavazzoni, MDApa itu Bamlanivimab?
Namanya mungkin sulit diucapkan, tetapi tujuan dari antibodi ini sederhana: "[The] protein buatan laboratorium meniru kemampuan sistem kekebalan untuk melawan antigen berbahaya seperti virus," kata FDA dalam rilisnya tentang bamlanivimab. </s> </s> </s> </s> </s> </s> </s> </s> </s> </s> </s> </s> </s> </s> </s> </s> </s> </s> </s> </s> </s> </s> </s> </s> </s> </s> </s> orang </s>
Pada dasarnya, bamlanivimab adalah campuran antibodi yang ditujukan untuk protein COVID-19, yang memungkinkannya menghentikan virus dari menempel dan memasuki sel manusia.
"Otorisasi darurat FDA atas bamlanivimab memberi para profesional perawatan kesehatan di garis depan pandemi ini dengan alat potensial lain dalam merawat pasien COVID-19," Patrizia Cavazzoni, MD, direktur pelaksana Pusat Evaluasi dan Penelitian Obat FDA, mengatakan di FDA's melepaskan. "Kami akan terus mengevaluasi data baru tentang keamanan dan kemanjuran bamlanivimab saat tersedia."
Baik Bamlanivimab Lilly dan REGN-COV2 Regeneron, koktail antibodi yang diterima Presiden Trump ketika dia didiagnosis dengan COVID-19, masih ditinjau. REGN-COV2, bagaimanapun, belum menerima EUA dari FDA.
Apa Perbedaan Antara EUA dan Persetujuan?
EUA tidak dimaksudkan untuk disamakan dengan persetujuan FDA.
"Dalam menentukan apakah akan mengeluarkan EUA, FDA mengevaluasi bukti yang tersedia dan dengan hati-hati menyeimbangkan risiko yang diketahui atau potensial dengan manfaat yang diketahui atau potensial dari produk untuk digunakan selama keadaan darurat," kata FDA dalam pernyataannya tentang bamlanivimab. "Berdasarkan tinjauan FDA terhadap totalitas bukti ilmiah yang tersedia, badan tersebut memutuskan bahwa masuk akal untuk percaya bahwa bamlanivimab mungkin efektif dalam merawat pasien yang tidak dirawat di rumah sakit dengan COVID-19 ringan atau sedang."
Dalam kasus EUA, "manfaat yang diketahui dan potensial lebih besar daripada risiko yang diketahui dan potensial untuk obat tersebut."
Apa berikutnya?
Pemerintah AS telah membeli 300.000 dosis bamlanivimab yang, menurut rilis berita Eli Lilly, tidak akan dikenakan biaya kepada orang Amerika (dengan pengecualian fasilitas perawatan kesehatan yang mungkin mengenakan biaya untuk pemberian obat tersebut).





-in-cancer.jpg)




-test.jpg)